Fusione e fissione nucleare
Parliamone un po’ .
“Fissione” deriva dal latino “fissionis”, che significa “fendere” oppure “dividere”, e quello che sto per dirti forse ti sorprenderà: escluso il nucleo dell’idrogeno-1, che è costituito solo da un protone, tutti i nuclei di tutti gli isotopi di tutti gli elementi sono fissionabili, dipende solo da quanta energia sei disposto a spendere!
Quello che cambia è il risvolto di tale fissione. Infatti esistono vari tipi di fissione:
- fissione endotermica non a catena
- fissione esotermica non a catena
- fissione esotermica a catena.
La fissione endotermica non a catena è quella che non produce energia, bensì la assorbe, e riguarda quasi tutti gli isotopi di tutti gli elementi più leggeri del rame. Ovviamente questo tipo di fissione non può essere usato per produrre energia!
La fissione esotermica non a catena è quella che invece produce energia, ma che non è in grado di autosostentarsi, quindi si arresta spontaneamente una volta rimossa la fonte d’innesco (tipo una sorgente neutronica). In questo caso sono in grado di prenderne parte sia nuclei pesanti che leggeri. A volte è richiesta un’energia neutronica spropositata, come per la fissione del bismuto, a volte serve un’energia intermedia, come per l’uranio-238, a volte è invece sufficiente una bassissima energia neutronica, come nel caso della fissione del litio-6:
⁶Li + n ➞ ⁴He + T -4,8 MeV
Questa reazione di fissione genera il 77% dell’energia della fissione dell’uranio-235 (a parità di massa), ma non genera neutroni per autosostentare la reazione, quindi non è una fissione a catena, seppur energetica.
Infine, la fissione esotermica a catena è invece quella che produce energia ma che è anche in grado di autosostentarsi, sia grazie ai neutroni che vengono liberati per ogni fissione (2–4), sia grazie a proprietà nucleari favorevoli (se vuoi approfondire, vedi la risposta lunga). Gli isotopi che permettono questo tipo di fissione, ovvero l’unica utilizzabile per produrre energia efficacemente, sono quelli detti fissili (fissionabili da neutroni di qualunque energia) oppure i fissibili (fissionabili da neutroni veloci). Ad oggi solo gli isotopi fissili sono o sono stati utilizzati per produrre energia (bombe atomiche incluse…) e i più importanti sono U-233, U-235, e Pu-239.
Tuttavia, nei reattori a neutroni veloci e nelle bombe termonucleari anche U-238 svolge un ruolo importante nella produzione di energia, anche se non da reazione a catena.
Passiamo ora alla fusione.
In questo caso le cose sono un po’ meno cervellotiche. Due nuclei si scontrano e si fondono in un unico nucleo più stabile, liberando energia. Tutti i nuclei sotto il ferro-56 sono in grado di produrre una fusione esotermica, ma la resa energetica per nucleone diminuisce velocemente aumentando la massa dei nuclei da fondere. Non solo! La reazione è tanto più difficile quanti più protoni ci sono nei nuclei, perché per poterli fondere occorre vincere la forza di repulsione tra le cariche positive dei protoni stessi. Quindi, ad esempio, la fusione dell’idrogeno-1 è più energetica di quella del carbonio-12 e richiede anche condizioni molto meno estreme, e così via. La fusione del deuterio e del trizio, entrambi isotopi dell’idrogeno, è meno energetica di quella dell’idrogeno-1 (fusione p-p), ma richiede temperature inferiori grazie ai neutroni extra nei loro nuclei che attenuano la repulsione tra i protoni (semplificazione estrema, ma in questa sede va benone).
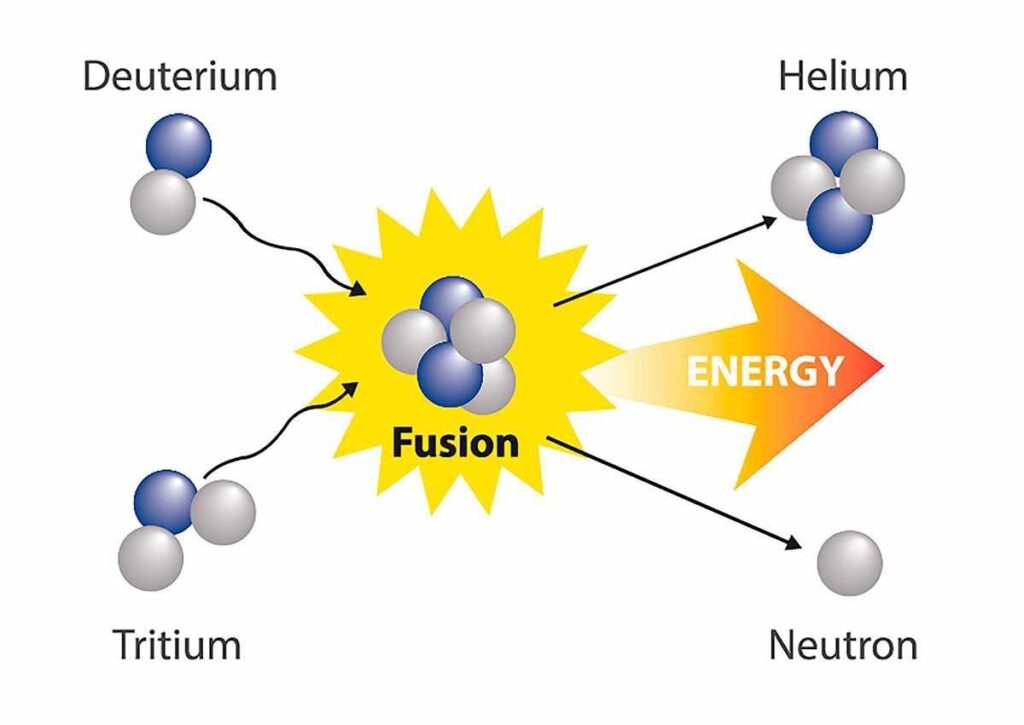
Invece, sopra il ferro-56 la fusione è sempre endotermica, quindi assorbe energia, richiedendo temperature mostruose e assolutamente irrealizzabili sulla Terra.
Curiosità: la fusione nucleare non è MAI una reazione a catena! Infatti, se nella fissione a catena ogni fissione innesca almeno un’altra fissione, nella fusione ogni evento è a sè stante, e non innesca altre fusioni. Certo, la temperatura aumenta e favorisce la fusione, ma senza un confinamento continuo la reazione si arresta spontaneamente.
Concludendo questa risposta breve, la fissione può essere fatta con tutti gli elementi, la fissione che produce energia solo con alcuni, mentre la fissione che produce energia e che si autoalimenta soltanto con gli elementi pesanti dal torio in poi, e solo con alcuni isotopi. Dal nettunio in poi però tutti gli isotopi sono fissili o fissibili, e quindi capaci di reazione a catena. La fusione può invece essere fatta con tutti gli elementi sotto il ferro-56, ma con gli elementi leggeri è sia molto più facile che molto più energetica, quindi tentare di fondere elementi più pesanti dell’elio non ha molto senso (eccetto casi molto particolari).
RISPOSTA LUNGA
Un nucleo atomico è formato da due tipi di particelle, i protoni, con carica positiva, e il cui numero determina l’elemento della tavola periodica, e i neutroni, senza carica, che fanno da “cuscinetto” per i protoni, e il cui numero determina l’isotopo di quell’elemento.
L’energia liberata dalle reazioni nucleari deriva dalla conversione in energia di una piccola frazione della massa iniziale, secondo la celeberrima formula einsteniana E=mc². In pratica, dopo la reazione, la somma delle masse dei prodotti è minore della massa del/dei nucleo/i o delle particelle di partenza. Questa massa mancante, che era presente nel nucleo sotto forma di energia di legame nucleare, viene appunto trasformata in energia.
La chiave del discorso è proprio la massa, o meglio, la differenza di massa. Poi capirai.
Ma ora focalizziamoci un attimo sulla fissione, ovvero la frammentazione del nucleo di un elemento in due o più nuclei più piccoli. E come funziona davvero la fissione? In pratica, un neutrone vagante colpisce un nucleo di un atomo, viene dapprima assorbito, e quindi il nucleo può fare due cose: tenerselo, e rimanere l’isotopo dello stesso elemento con un neutrone in più, oppure spaccarsi in due, ovvero fissionarsi. Ma ovviamente ogni isotopo di ogni elemento reagirà in maniera diversa, proprio per le sue intrinseche proprietà nucleari. Alcuni isotopi si fissionano facilmente, altri invece no, preferendo tenersi il neutrone. Alcuni isotopi si fissionano solo con neutroni veloci, altri anche con neutroni lenti. Alcuni isotopi possono (o potrebbero teoricamente) essere usati per costruire ordigni nucleari, altri no, e per capire cosa sta alla base di questi comportamenti così diversi è necessario introdurre due altri concetti molto importanti: la barriera di fissione nucleare, e l’energia di legame del neutrone. Tranquillo, ora ti spiego tutto nel modo più semplice e chiaro possibile.
La barriera di fissione nucleare è banalmente l’energia che bisogna fornire al nucleo di un certo isotopo per indurlo a fissionarsi. Queste energie, tutte tabulate e reperibili online (alcune sperimentali, molte calcolate), sono diverse da elemento a elemento e da isotopo a isotopo, ma mostrano un trend caratteristico. Infatti diminuiscono mano a mano che si scende lungo la tavola periodica, aumentando quindi il numero di protoni e neutroni, e quindi la massa dei nuclei atomici. Detto in poche parole, più l’elemento è pesante, e minore sarà l’energia necessaria per fissionarlo. Tali energie vengono espresse in eV(elettronvolt) e suoi multipli. Ad esempio, per fissionare il bismuto-209 servono circa 24 MeV (Megaelettronvolt, ovvero 1 milione di eV), per il radon-222 servono circa 10 MeV, per il radio-226 servono 8 MeV, per il torio-232 ne servono 7, e così via. Questa energia viene fornita al nucleo in due modi: tramite l’energia cinetica del neutrone in arrivo (la sua velocità), sempre espressa in eV o multipli, e tramite l’energia di legame del neutrone. Ma che cosa sarà mai questa strana energia?
È proprio qui che entra in gioco la differenza di massa di cui parlavo prima.
Vediamo l’esempio della fissione dell’uranio-235, per capire meglio. Come dicevo prima, il neutrone in arrivo viene prima assorbito, trasforma l’uranio-235 in uranio-236, poi l’uranio-236 (in uno stato eccitato) può o fissionarsi oppure perdere l’energia in eccesso tramite un fotone energetico (raggio gamma).
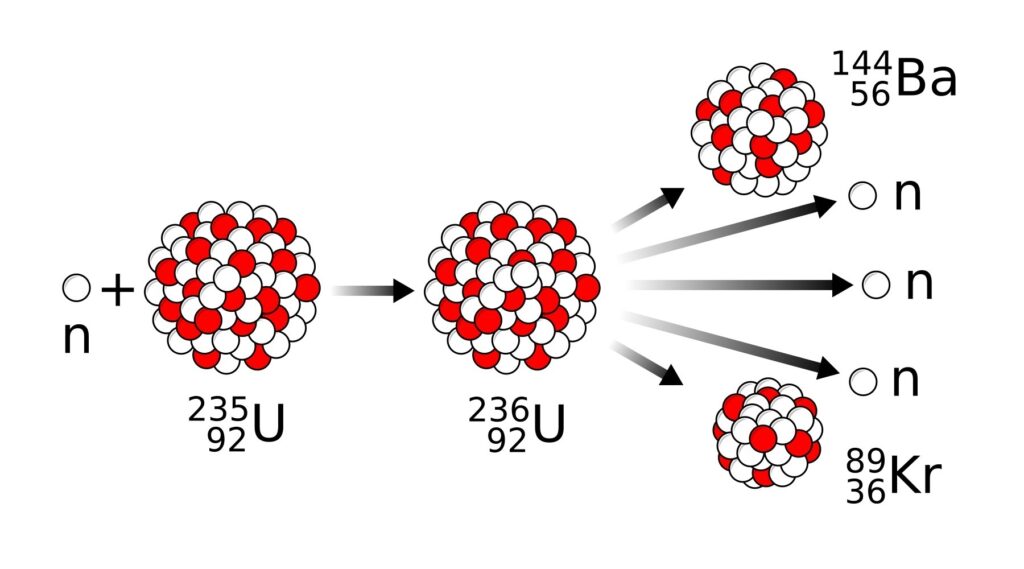
Per trovare il contributo energetico derivante dall’energia di legame del neutrone dobbiamo sapere i valori delle masse nucleari esatte dei due isotopi dell’uranio coinvolti. Quindi le masse esatte, in dalton (Da), sono:
U-235 = 235,043928 Da
U-236 = 236,045566 Da
Ma per la reazione U-235 + neutrone (n) ci serve sapere anche la massa di quest’ultimo, che vale:
n = 1,00866491588 Da
Mi raccomando! Qui non si fanno arrotondamenti! Più cifre usi dopo la virgola e meglio è.
Se fai la somma delle masse di U-235 e di n viene fuori:
U-235 + n = 236,05259291588 Da
Non noti nulla? Se guardi bene, quest’ultima somma ci restituisce un valore di massa leggermente superiore al valore di massa tabulato per U-236. Questo significa che il nucleo di U-236 appena nato ha un po’ di massa extra, massa che va rimossa sotto forma di energia per ottenere un nucleo di U-236 stabile. Se calcoli questa differenza di massa tra l’U-236 eccitato e l’U-236 stabile e la moltiplichi per l’energia equivalente contenuta in un’unità di massa (1 Da = 931,49410242 MeV), ottieni che l’energia extra dell’U-236 eccitato equivale a 6,54 MeV. Questa è precisamente l’energia di legame del neutrone! In altre parole, è l’energia che bisogna fornire ad un nucleo di U-236 per strappargli via un neutrone.
E ora torna in campo la barriera di fissione nucleare. Come ho spiegato prima, per indurre un nucleo di U-236 alla fissione serve una certa quantità di energia. Per questo specifico nucleo la barriera sperimentale per la fissione vale 5,67 MeV. Ora, siccome questa barriera è minore dell’energia extra del nucleo di U-236 appena nato (che vale 6,54 MeV) già per il semplice fatto di aver assorbito un neutrone, è chiaro che a questo punto il nucleo di U-236 eccitato può fissionarsi indipendentemente dalla velocità (e quindi dall’energia) del neutrone in arrivo. Quindi, se per un qualunque nucleo la differenza tra l’energia di legame del neutrone (dopo assorbimento di n) e la barriera di fissione nucleare (sempre dopo assorbimento di n) è un valore maggiore di zero, l’isotopo del nucleo di partenza (prima di assorbire il neutrone) viene detto FISSILE, e quindi può fissionarsi con neutroni di qualunque velocità. Se invece tale differenza è minore di zero, l’isotopo viene detto FISSIONABILE, e quindi può fissionarsi con neutroni che siano abbastanza veloci da colmare il gap energetico tra l’energia di legame del neutrone e la barriera di fissione nucleare.
Nota: “fissionabile” vuol dire tutto e niente, visto che è possibile fissionare praticamente qualunque isotopo di qualunque elemento della tavola periodica, dipende solo da quanta energia puoi dare al neutrone.
Ma comunque non tutti gli isotopi fissionabili sono uguali. Facciamo un passo indietro. Tutti i nuclei pesanti sono soggetti a fissione spontanea, che avviene senza aggiungere energia al sistema (per effetto tunnel). Quando un nucleo si fissiona, fissile o fissionabile che sia, si scinde in almeno due nuclei più leggeri, e contemporaneamente libera 2–4 neutroni. Questi neutroni, che hanno un’energia media di circa 2 MeV, possono colpire altri nuclei vicini e indurli alla fissione. Con piccole quantità di materiale questa fissione spontanea è innocua e non si propaga più di tanto ai nuclei vicini. Mettendo però insieme una certa quantità di materiale fissile o fissionabile, si arriva ad una certa massa (stavolta in kg!) oltre la quale le reazioni di fissione si automoltiplicano, causando una reazione di fissione a catena incontrollata e, nelle giuste condizioni, un’esplosione nucleare. Questa massa viene chiamata massa critica, ed è diversa per ogni isotopo.
Ma chiaramente non tutti gli isotopi hanno massa critica! Una cosa però è certa: tutti gli isotopi fissili hanno sicuramente una massa critica. Ad esempio l’uranio-235 ha una massa critica di circa 47 kg, l’uranio-233 ce l’ha di circa 16 kg, e il plutonio-239 di 10kg (tutti i valori si riferiscono a sfere piene non schermate). Tuttavia esistono anche molti isotopi non fissili che hanno ugualmente una massa critica. Infatti, per avere una massa critica, la fissilità è una condizione sufficiente ma non necessaria. Negli anni ‘80 è stato proposto il termine “fissibile” per indicare tutti gli isotopi non fissili ma con massa critica, ma non è stato ancora accettato dalla comunità scientifica (io lo uso comunque, visto che è comodo per il discorso). Di isotopi fissibili ce ne sono davvero tanti, come: il torio-229, l’uranio-234, il nettunio-237, il plutonio-238 e il 240, ecc ecc. Questi isotopi possono dare luogo a fissione a catena esplosiva perché il gap energetico tra l’energia di legame del neutrone e la barriera di fissione nucleare è abbastanza piccolo da essere facilmente colmato dall’energia di 2 MeV dei neutroni prodotti dalla fissione.
Ma non basta ancora. Ci sono infatti degli isotopi che, nonostante il gap piccolo, non possono dare origine ad una fissione a catena, in nessuna condizione. Questo dipende da un’altra proprietà nucleare, ovvero lo scattering anelastico, che causa una perdita di energia dei neutroni mentre rimbalzano tra i nuclei di quell’isotopo. Perdendo energia diventano quindi troppo lenti per colmare il gap energetico per far fissionare un altro nucleo, e la reazione a catena muore velocemente. Alcuni degli isotopi più rappresentativi di questa ultima categoria sono: l’attinio-227, il torio-230 e il 232, il protoattinio-231, l’uranio-236 e il 238. Lo scattering anelastico é presente anche per gli isotopi fissili, solo che questi nuclei non è un problema, visto che l’energia dei neutroni non ne influenza la fissibilità. Gli isotopi come l’uranio-238 non possono quindi essere usati come esplosivi nucleari primari, e possono essere stoccati in quantità illimitate senza problemi, dal momento che non hanno massa critica.
Tuttavia, la fissione di questi isotopi “innocui” indotta da neutroni molto energetici (come quelli da 14 MeV prodotti dalla fusione nucleare delle bombe H) è comunque molto energetica! Infatti l’energia generata dalla fissione è indipendente da tutti i parametri energetici citati prima, e anche la fissione dell’U-238 genera circa la stessa energia per kg derivata dalla fissione di isotopi fissili quali l’U-235 e il Pu-239. L’uranio-238 può essere usato quindi come stadio terziario delle bombe termonucleari (fissione a catena-fusione-fissione indotta), e siccome per lui non ci sono limiti di massa può essere aggiunto anche a tonnellate. In questi casi, il 75–80% della potenza esplosiva totale deriva proprio dalla fissione indotta dell’U-238.
Infine, sommando tutti i parametri nucleari viene fuori un parametro importantissimo, chiamato K(infinito). Questo numero, diverso per ogni isotopo, ci dice se quell’isotopo ha o non ha massa critica, e ci da anche un’idea di quanto sia grande. In pratica è il valore di moltiplicazione delle reazioni di fissione a catena calcolato per una massa infinita di materiale (per evitare di perdere neutroni preziosi nell’ambiente). Se la K(inf.) vale 2, ad esempio, ogni fissione causerà in media altre due fissioni, se vale 3, altre tre fissioni, e via dicendo. Più la K(inf.) è grande e maggiore di 1 e minore sarà la massa critica. Ad esempio, l’U-233 ha una K(inf.) di 2,56 e una massa critica di 16 kg, l’U-235 ha una K(inf.) di 2,28, e la massa critica sale a 47 kg. Il nettunio-237 ha una K(inf.) di 1,7, e la massa critica sale a 64 kg. L’uranio-234 ha una K(inf.) di appena 1,5, e la sua massa critica è di ben 145 kg. Se invece la K(inf.) è minore o uguale a 1 l’isotopo in questione non avrà massa critica. Ad esempio l’U-238 ha una K(inf.) di 0,34, l’U-236 di 0,74, e il Th-232 di 0,08, e non sono quindi isotopi che possono dare origine a una fissione a catena esplosiva.
Quindi, per capire quali isotopi sono fissili e quali no, perlomeno sulla carta, è molto semplice: basta sottrarre il valore della barriera di fissione (dell’isotopo +1) all’energia di legame del neutrone (sempre dell’isotopo +1). Ricorda che sono tutti valori facilmente reperibili online gratuitamente. Identificare un isotopo fissibile è invece molto più difficile, perché il calcolo della K(inf.) non è una cosa semplicissima.
Per mia curiosità personale ho fatto tutti i conti con le barriere energetiche e con l’energia di legame del neutrone, e questo è quello che è venuto fuori:
- Nessun elemento dal polonio all’attinio (polonio, astato, radon, francio, radio, attinio) ha isotopi fissili, semplicemente perché le barriere di fissione sono troppo grandi.
- L’elemento più leggero con isotopi fissili è il torio, e ne ha tre (227, 231, 233).
- Il protoattinio ne ha ben 9 (220, 222, 224, 226, 228, 229, 230, 232, 234).
- L’uranio ne ha almeno 14 (dal 221 al 233, 235).
- Il nettunio almeno 15 (dal 222 al 234, 236, 238).
- Il plutonio anche lui almeno 14 (dal 227 al 237, 239, 241, 243).
- Gli elementi più pesanti si comportano in modo molto simile al plutonio.
Tuttavia, anche se gli isotopi che secondo i calcoli potrebbero produrre una reazione di fissione a catena sono diverse decine, nella pratica sono soltanto tre (U-233, U-235, Pu-239) gli isotopi fissili che possono essere usati per produrre energia, sia per una questione di reperibilità/sintetizzabilità, che per una questione di tempo di decadimento/radioattività. L’uranio-233 può essere prodotto dal torio-232, l’uranio-235 è già presente in natura (allo 0,72% nell’uranio naturale), e il plutonio-239 viene prodotto dall’uranio-238. Tutti gli altri isotopi fissili sono invece troppo instabili, e spesso pure difficilissimi e costosissimi da produrre e/o estrarre dal combustibile esausto, e quindi non vengono utilizzati (il nettunio-237 potrebbe essere usato nei reattori a neutroni veloci, ma va estratto dal combustibile esausto, una pratica molto costosa). Nei reattori veloci anche U-238 e Th-232 contribuiscono a produrre energia per fissione diretta, anche se non possono essere usati da soli visto che non hanno massa critica.

