Nel cuore della cellula: nuove intuizioni sull’utilizzo di farmaci basati sulla nanotecnologia
I nuovi farmaci, come i vaccini contro il COVID-19, tra gli altri, si basano sul trasporto di farmaci mediante nanoparticelle. Per molto tempo non è stato chiarito se questo trasporto del farmaco sia influenzato negativamente da un accumulo di proteine del sangue sulla superficie della nanoparticella.
Gli scienziati del Max Planck Institute for Polymer Research hanno ora seguito il percorso di una tale particella all’interno di una cellula utilizzando una combinazione di diversi metodi di microscopia. Sono stati in grado di osservare un processo interno alla cellula che separa efficacemente i componenti del sangue e le nanoparticelle .
Le nanoparticelle sono un campo di ricerca attuale ed è impossibile immaginare la medicina moderna senza di esse. Servono come microscopiche capsule di farmaci che hanno un diametro inferiore a un millesimo di millimetro. Tra le altre cose, vengono utilizzati negli attuali vaccini contro il COVID-19 per fornire efficacemente i principi attivi dove sono effettivamente necessari. Nella maggior parte dei casi, le capsule si agganciano alle cellule, ne sono avvolte e vengono assorbite in esse. All’interno della cellula, i processi chimici possono quindi aprire le capsule, rilasciando il principio attivo.
Tuttavia, questo processo idealizzato di solito non ha luogo: mentre viaggia attraverso il flusso sanguigno, le proteine del sangue si accumulano sulla superficie del nanotrasportatore. Anche questi trovano la loro strada nella cella. Per molto tempo è stata una questione irrisolta se questo processo comprometta il rilascio del principio attivo.
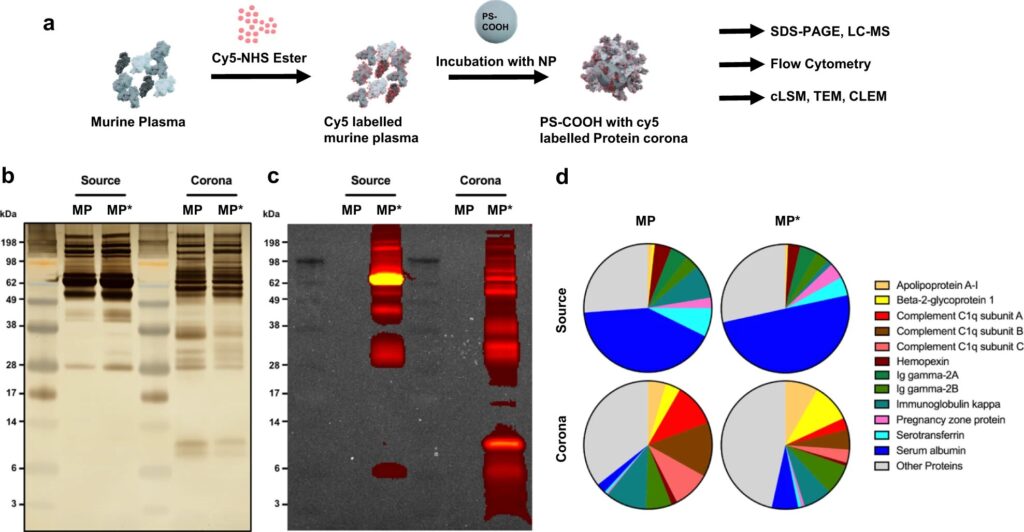
Gli scienziati che lavorano con Ingo Lieberwirth, capogruppo nel dipartimento di Katharina Landfester, hanno ora affrontato questa domanda. Hanno etichettato una nanoparticella e proteine del sangue con diversi coloranti fluorescenti. Di conseguenza, entrambi brillano di colori diversi se osservati attraverso un microscopio ottico ad alta risoluzione. Allo stesso tempo, i ricercatori sono stati in grado di osservare il processo in parallelo ea una risoluzione maggiore utilizzando un microscopio elettronico .
Combinando entrambi i metodi, gli scienziati sono stati in grado di osservare che la cellula inizialmente assorbe il composto di nanoparticelle e proteine del sangue. Nella cellula, ora hanno osservato qualcosa di sorprendente: il rivestimento proteico si stacca dalla nanoparticella e la rilascia. Dopo un po’ di tempo, le proteine e le particelle sono presenti separatamente nella cellula.
“Supponiamo quindi che il rilascio del farmaco nella cellula non sia disturbato dal rivestimento proteico”, afferma Ingo Lieberwirth. “Tuttavia, ora è importante scoprire come avviene esattamente il processo all’interno della cellula”.
Gli scienziati hanno ora pubblicato i loro risultati su Nature Communications .

